Pendahuluan
Listrik dapat dibuat ketika bahan kimia tertentu bereaksi bersama-sama. Kita biasanya menggunakan bahan kimia untuk membuat listrik misalnya pada lampu senter, baterai sebuah jam atau kadang-kadang baterai mobil. Ya, ada mobil yang berjalan di listrik! Perangkat yang menyimpan listrik disebut baterai. Sebaliknya listrik juga dapat digunakan untuk menghasilkan perubahan kimia atau yang disebut proses Elektrolisis.
Air adalah bahan kimia sederhana yang terbuat dari dua gas yaitu hidrogen dan oksigen. Setiap molekul air memiliki dua atom hidrogen untuk setiap atom oksigen. H2O adalah rumus kimia untuk molekul air.
 |
| Model kimia Air |
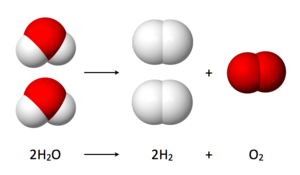
Jika arus listrik dilewatkan melalui air antara elektroda (positif dan negatif dari kutub baterai), maka air akan dibagi menjadi dua bagian yang: oksigen dan hidrogen. Proses ini disebut elektrolisis dan digunakan dalam industri dalam banyak hal, seperti membuat logam seperti aluminium. Jika salah satu dari elektroda adalah logam, maka logam tersebut itu akan menjadi tertutup atau berlapis dengan logam dalam larutan. atau yang disebut dengan proses Elektroplanting atau penyepuhan.
Kita dapat menggunakan listrik untuk membuat gas hidrogen dari air mirip dengan proses yang disebut elektrolisis.
Alat Dan Bahan
Sebuah baterai 9 volt (bisa menyusun baterai 1,5 Volt)
Dua batang pensil
Garam
Kardus Tipis
Kabel
Gelas kecil
Air
Langkah Kerja
1. Tajamkan kedua ujung pensil.
2. Potong kardus sesuai dengan ukuran gelas.
3. Masukan dua pensil ke dalam kardus, sekitar satu inci terpisah.
4. Larutkan sekitar satu sendok teh garam ke dalam air hangat dan diamkan selama beberapa saat. Garam membantu menghantarkan listrik lebih baik dalam air.
5. Salah satu bagian dari salah satu ujung kabel dihubungkan pada sisi positif dari baterai dan yang ujung kabel lain untuk grafit hitam di bagian atas pensil. Lakukan hal yang sama untuk sisi negatif menghubungkannya ke atas pensil kedua.
6. Tempatkan kedua ujung lain dari pensil ke dalam air asin.

Hasil Dan Pembahasan
Arus listrik dari baterai melewati diantara dua elektroda (pensil), air terbagi menjadi hidrogen dan gas klor, yang mengumpulkan gelembung sebagai sangat kecil di sekitar masing-masing ujung pensil.
Hidrogen mengumpul disekitar katoda (kutub negatif) dan gas klorin mengumpulkan sekitar anoda (kutub positif).
Bagaimana kita bisa mendapatkan klorin dari H2O? Karena dalam percobaan ini kita menggunakan garam maka gas klor keluar dari garam tersebut atau NaCl
Oksigen tidak dapat keluar percobaan ini. Itu karena atom oksigen dari air menggabungkan dalam cairan dengan garam untuk membentuk ion hidroksil. Rumus kimia garam adalah NaCl atau natrium klorida. Gas klorin dari klorida dalam garam. Oksigen dalam ion hidroksil tinggal dalam larutan. Jadi, apa yang terjadi pada reaksi ini tidak oksigen tetapi gas klorin yang mengumpulkan sekitar ujung pensil. Sekitar pensil lainnya adalah gas hidrogen.
Untuk membuat Oksigen dari air dengan cara ini bisa menggunakan air tanpa garam atau menggunakan aquades, tapi tentu saja proses elektrolisisnya tidak secepat bila menggunakan garam sebagai membantu penghantar listrik dalam air
